Contenidos
MIELOPATÍA TRAUMÁTICA Y MIELOPATÍAS DESMIELINIZANTES
MIELOPATÍA TRAUMÁTICA
Aunque el daño medular puede deberse a una lesión por latigazo (extensión cervical), un daño grave a la médula normalmente se relaciona con fractura-luxación en la región cervical, torácica inferior o lumbar superior.
Hallazgos clínicos
- Transección medular total
Una transección total ocasiona una inmediata parálisis permanente y pérdida de sensación por debajo del nivel de la lesión. Aunque la actividad refleja se pierde durante un periodo variable después del daño, más adelante hay un aumento persistente en la función refleja.
- En la etapa aguda, se presenta una parálisis flácida con pérdida de reflejos tendinosos y de otro tipo, acompañada de pérdida sensorial y de retención urinaria y fecal. Ésta es la etapa del choque espinal.
- A lo largo de las siguientes semanas, a medida que se restaura la función refleja, surge el cuadro clínico de una paraplejia o cuadriplejia espástica, con reflejos tendinosos enérgicos y respuestas de extensión plantar; sin embargo, una parálisis flácida y atrófica (de neurona motora inferior) puede afectar a los músculos inervados por segmentos de la médula espinal al nivel de la lesión, donde se encuentra el daño a las células del asta anterior. Ahora, la vejiga y los intestinos recuperan cierta función refleja, de modo que la orina y las heces se expulsan a intervalos.
- Los espasmos flexores o extensores de las piernas pueden volverse cada vez más problemáticos y a la larga se ven evocados incluso por el estímulo cutáneo más leve, sobre todo en presencia de llagas por presión o de infección del tracto urinario. A la larga, el paciente asume una postura con las piernas en flexión o extensión, siendo la primera la más probable en el caso de lesiones cervicales o medulares totales.
- Lesiones menos graves
En los casos en que el grado de daño es menor, la deficiencia neurológica es menos grave y menos total, pero es posible que los pacientes queden con una paraparesia o cuadriparesia leve o con alteraciones sensoriales distales. También es posible que la función esfinteriana quede comprometida; la urgencia urinaria y la incontinencia por urgencia son en especial comunes. Las lesiones por hiperextensión del cuello pueden conducir a una isquemia medular focal que ocasiona paresia bibraquial (debilidad de ambos brazos) sin afectación de las piernas y signos sensoriales variables.
Tratamiento
- Inmovilización
El tratamiento inicial consiste en inmovilización hasta que se determina la naturaleza y amplitud de la lesión. Si existe compresión medular, será necesaria una urgente cirugía de descompresión. Es posible que una columna inestable requiera de fijación quirúrgica y que las luxaciones vertebrales requieran de tracción.
- Corticosteroides
Los corticosteroides (p. ej., metilprednisolona, 30 mg/kg, bolo intravenoso, seguido de infusión intravenosa de 5.4 mg/kg/h durante 24 horas) pueden mejorar la función motora y sensorial a los seis meses cuando el tratamiento se inicia dentro de las ocho horas próximas al traumatismo de la médula espinal, aunque análisis recientes de evidencia publicada arrojan dudas sobre cualesquiera efectos benéficos significativos. El mecanismo de acción es desconocido, pero existe la posibilidad de que implique la inhibición de la peroxidación de lípidos y la mejoría de la irrigación sanguínea a la médula lesionada.
- Espasmos dolorosos
Los dolorosos espasmos flexores o extensores se pueden tratar con medicamentos que aumenten los mecanismos inhibitorios medulares (baclofen, diacepam) o que desacoplen la excitación muscular de la contracción (dantroleno). Deben administrarse 5 mg de baclofen por vía oral, dos veces al día y hasta 30 mg cuatro veces al día; diacepam, 2 mg vía oral, dos veces por día y hasta 20 mg, tres veces por día; y dantroleno, 25 mg/d, vía oral y hasta 100 mg, cuatro veces al día. La tizanidina, un agonista α2-adrenérgico central, también puede resultar de utilidad, pero es poco claro su mecanismo preciso de acción.
La dosis diaria se aumenta de manera gradual, por lo general a 8 mg, tres veces por día. Los efectos secundarios incluyen resequedad de boca, somnolencia e hipotensión, pero el fármaco es bien tolerado en general. Los pacientes que no se beneficien de los medicamentos orales o que no puedan tolerar dosis suficientes de estos medicamentos posiblemente respondan a una infusión intratecal de baclofen.
Todos estos medicamentos pueden aumentar la discapacidad funcional al reducir el tono. También es posible que el dantroleno aumente la debilidad y debe evitarse en pacientes cuya función respiratoria esté gravemente comprometida.
- Cuidados de la piel
Debe prestarse particular atención al cuidado de la piel y evitarse una presión continua sobre cualquier área específica.
- Trastornos urinarios e intestinales
En función de la gravedad de la lesión, es posible que sea necesario llevar a cabo una cateterización inicial. Más adelante, es posible que la urgencia y frecuencia de la vejiga espástica respondan a un fármaco parasimpaticolítico como oxibutinina, 5 mg, tres veces por día. Los supositorios y enemas ayudarán a mantener un funcionamiento intestinal regular y pueden prevenir o controlar la incontinencia fecal.
- Terapéutica experimental
En épocas recientes, el trabajo experimental se ha enfocado en intensificar la regeneración axonal en la sección dañada de la médula espinal por medio de abordajes tales como la neutralización de la inhibición de neuritas, el uso de factores neurotróficos o de crecimiento, la implantación de canales sintéticos y las terapias celulares. En el futuro próximo es probable que se realice una aplicación traslacional a pacientes con lesiones de la médula espinal.
MIELOPATÍAS DESMIELINIZANTES
Esclerosis múltiple
Epidemiología
- La esclerosis múltiple es uno de los trastornos neurológicos más comunes, afecta a unos 300000 pacientes en Estados Unidos y su máxima incidencia se encuentra entre jóvenes adultos.
- Por lo general, los síntomas iniciales comienzan antes de los 55 años de edad, con una incidencia máxima entre las edades de 20 y 40 años; las mujeres se ven afectadas casi al doble que los varones.
Patología
El trastorno se caracteriza patológicamente por el desarrollo de áreas focales dispersas a menudo perivenulares de desmielinización seguida de una gliosis reactiva; también es posible que haya daño axonal. Estas lesiones suceden en la materia blanca del cerebro y de la médula y dentro del nervio óptico (II).
Fisiopatología
- Se desconoce la causa de la esclerosis múltiple, pero se cree que el daño a los tejidos y los síntomas neurológicos son el resultado de un mecanismo inmunológico dirigido en contra de los antígenos de la mielina. Es posible que las infecciones virales y otros factores instigadores promuevan la entrada de células T y de anticuerpos en el SNC al perturbar la barrera hematoencefálica.
- Esto conduce a una expresión aumentada de moléculas de adhesión celular, metaloproteinasas de matriz y citocinas proinflamatorias, que trabajan en concierto para atraer células inmunitarias adicionales, romper la matriz extracelular para ayudar a su migración y activar respuestas autoinmunitarias en contra de antígenos tales como proteína básica de mielina, glucoproteína asociada a mielina, glucoproteína oligodendrocitaria de mielina, proteína proteolípida, αB-cristalina, fosfodiesterasas y S-100.
- El enlace de estos antígenosblanco por células presentadoras de antígenos detona una respuesta autoinmunitaria que puede involucrar citocinas, macrófagos y complemento. El ataque inmunológico sobre la mielina denuda a los axones, lo que reduce la conducción nerviosa y conduce a síntomas neurológicos.
Hallazgos clínicos
- Síntomas iniciales o de presentación
- Los pacientes pueden presentarse con cualquiera de una variedad de síntomas. Las afecciones iniciales comunes son debilidad focal, entumecimiento, hormigueo o inestabilidad en alguna extremidad; pérdida repentina o confusión de la visión en un ojo (neuritis óptica); diplopía; desequilibrio; o una alteración de la función urinaria (urgencia o vacilación urinarias).
- A menudo, estos síntomas son transitorios y desaparecen después de unos cuantos días o semanas, aun cuando es posible encontrar alguna deficiencia residual después de un cuidadoso examen neurológico. Otros pacientes presentan una paraparesia espástica aguda o gradualmente progresiva y deficiencias sensoriales; esto debería despertar preocupación en cuanto a la posibilidad de alguna lesión estructural subyacente a menos que haya evidencia, bajo examen clínico, de enfermedad más generalizada.
- Curso subsiguiente
- Es posible que haya un intervalo de meses o años después del episodio inicial antes de que aparezcan más síntomas neurológicos. Entonces, existe la posibilidad de que se desarrollen nuevos síntomas, o puede haber una recurrencia y progreso de los síntomas originales. Las recaídas pueden ser precipitadas por infección y, en el caso de las mujeres, son más probables alrededor de los tres meses después de un parto (pero se reducen durante el embarazo en sí).
- Un aumento en temperatura corporal puede ocasionar un deterioro transitorio en pacientes con una deficiencia fija y estable. Al paso del tiempo y después de varias recurrencias y de remisiones por lo general incompletas es posible que el paciente se vea cada vez más incapacitado por debilidad, rigidez, alteraciones sensoriales inestabilidad de las extremidades, trastornos visuales e incontinencia urinaria.
Estudios de investigación
Por lo general, el líquido cefalorraquídeo (LCR) es anormal, con una linfocitosis leve o una concentración proteínica ligeramente aumentada, en especial si se examina poco después de una recaída aguda. La electroforesis de proteínas en el LCR muestra la presencia de bandas discretas en la región (IgG) de inmunoglobulina G (bandas oligoclonales) en 90% de los pacientes. Se desconocen los antígenos responsables de estos anticuerpos.
- Si existe evidencia clínica de lesión sólo en un sitio del SNC, no se puede hacer un diagnóstico apropiado de esclerosis múltiple a menos que otras regiones se hayan visto afectadas de manera subclínica, según se haya detectado por medio de las respuestas electrocerebrales evocadas por una o más de las siguientes señales: estimulación visual monocular con un patrón de tablero de ajedrez (potenciales evocados visuales); estimulación monoaural con chasquidos repetitivos (potenciales evocados auditivos de tronco encefálico); y estimulación eléctrica de un nervio periférico (potenciales evocados somatosensoriales).
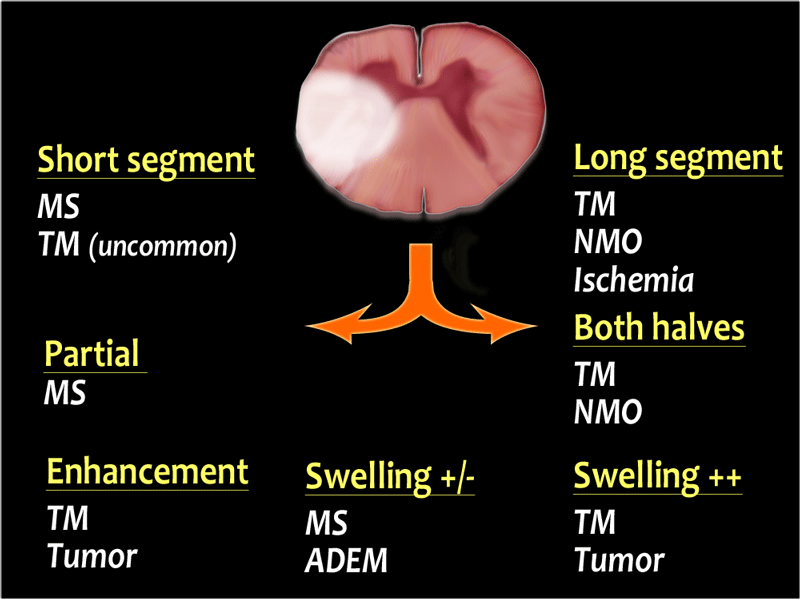
- La IRM también puede detectar lesiones subclínicas y se ha vuelto prácticamente indispensable para la confirmación del diagnóstico, como se detalla en la siguiente sección acerca del diagnóstico. Las imágenes potenciadas en T1 pueden revelar “agujeros negros” hipointensos que probablemente representen áreas de daño axonal permanente; también se encuentran lesiones hiperintensas. Las imágenes en T1 con captación de gadolinio pueden destacar áreas de inflamación con una afectación de la barrera hematoencefálica.
- Las imágenes potenciadas en T2 proporcionan información acerca de la carga de enfermedad o carga lesional (es decir, número total de lesiones) que de manera típica aparecen como áreas de alta intensidad de señal. Otros cambios en la IRM, incluyendo medidas de atrofia cerebral, imágenes de transferencia de magnetización, espectroscopia por resonancia magnética e imágenes con tensor de difusión seguramente proporcionarán información aún más pertinente.
- En ocasiones una IRM de sujetos saludables muestra “objetos brillantes no identificados” que se asemejan a las lesiones de la esclerosis múltiple. Por lo general no tienen correlatos ni significado clínico pero en ocasiones pueden ser biomarcadores tempranos de la enfermedad. Por ende, los hallazgos de imagenología deben interpretarse dentro del contexto clínico en el que se obtuvieron.
- En el caso de pacientes que se presentan con la forma espinal del padecimiento y sin evidencia de diseminación de la enfermedad, es posible que sea necesario llevar a cabo una IRM o mielografía espinal a fi n de excluir la posibilidad de una lesión sencilla congénita o adquirida quirúrgicamente que sea tratable.
- Debe visualizarse la región del foramen magno a fin de excluir la posibilidad de una lesión tal como una malformación de Arnold-Chiari, en la que parte del cerebelo y del tronco encefálico inferior se desplazan hacia el canal cervical, produciendo deficiencias piramidales y cerebelosas mixtas en las extremidades.
Diagnóstico
El diagnóstico de esclerosis múltiple requiere de evidencia de que al menos dos regiones distintas de materia blanca central se hayan visto afectadas en momentos diferentes. Una enfermedad clínicamente definitiva se puede diagnosticar en pacientes con un curso recurrente-remitente y signos de al menos dos lesiones que afecten regiones distintas de materia blanca central. Se diagnostica una probable esclerosis múltiple cuando los pacientes muestran evidencia de enfermedad multifocal de materia blanca, pero que han tenido sólo un ataque clínico o que tienen antecedentes de al menos dos episodios clínicos pero con una sola lesión.
- Se pueden utilizar las imágenes para mostrar la diseminación en el tiempo si existe una lesión con captación de gadolinio al menos tres meses después del principio del suceso clínico inicial en un sitio diferente al que corresponde al suceso inicial o si se encuentra una nueva lesión T2 en cualquier momento cuando se compara con una exploración de línea base obtenida al menos 30 días después del suceso clínico inicial.
- La diseminación en espacio requiere tres de las siguientes lesiones:
- Al menos una lesión con captación de gadolinio o nueve lesiones hiperintensas en T2 si no existe una lesión con captación;
- Una o más lesiones infratentoriales (o de la médula espinal)
- Una o más lesiones yuxtacorticales;
- Al menos tres lesiones periventriculares.
- El diagnóstico de enfermedad progresiva primaria requiere, además de un año de progresión de la enfermedad, dos de los siguientes datos:
- Una IRM positiva (nueve lesiones en T2 o al menos cuatro lesiones en T2 con un potencial evocado visual anormal);
- Dos o más lesiones focales en T2 en una IRM espinal;
- LCR positivo (bandas oligoclonales, aumento en el índice de IgG, o ambas).
Tratamiento
En los pacientes con enfermedad recurrente-remitente, el tratamiento indefinido con interferón β-1a o con interferón β-1b en un régimen de dosis que depende de la formulación reduce la frecuencia de las recurrencias. El acetato de glatiramer (anteriormente copolímero 1, una mezcla aleatoria de polímeros que simulaban la composición de aminoácidos de la proteína básica de mielina) administrado por medio de inyección subcutánea diaria parece ser igual de efectivo.
- Además de su efecto sobre las recaídas, el interferón β-1a y el acetato de glatiramer también pueden demorar el inicio de discapacidad significativa en pacientes con enfermedad recurrente. El natalizumab, un antagonista de la integrina α-4, reduce la tasa de recaídas, pero en raras ocasiones se ha asociado con el desarrollo de leucoencefalopatía multifocal progresiva.
- Es posible que las infusiones intravenosas con inmunoglobulina (IVIg) también reduzcan la frecuencia de recaídas en la enfermedad recurrente-remitente, pero las recomendaciones de tratamiento son prematuras. En ocasiones, la plasmaféresis es de utilidad cuando los pacientes tienen recaídas graves que no responden a los esteroides.
- Los efectos secundarios más comunes de los interferones son un síndrome catarral y (en el caso del interferón β-1b) reacciones en el sitio de inyección. El acetato de glatiramer por lo general es bien tolerado, pero puede producir eritema en el sitio de inyección y cerca de 15% de los pacientes experimentan episodios transitorios de rubefacción, disnea, opresión en el pecho, palpitaciones y ansiedad después de las inyecciones.
- Los tres agentes están aprobados para su uso en esclerosis múltiple recurrente-remitente y están disponibles mediante receta médica. Son costosos, pero su precio debe equilibrarse contra la reducción en la necesidad de cuidados médicos y la menor pérdida de tiempo laboral que ocasiona su uso.
- Los corticosteroides pueden acelerar la recuperación de recaídas agudas, pero el grado de la recuperación misma no cambia. La administración de esteroides a largo plazo no evita las recaídas y no debería utilizarse a causa de sus efectos colaterales inaceptables. No existe un programa estandarizado de tratamiento con corticosteroides, pero el régimen más ampliamente utilizado es de metilprednisolona intravenosa (1 g diario) durante tres a cinco días, seguido de una disminución gradual de prednisona oral (1 mg/kg/d durante una semana, seguida de una rápida reducción a lo largo de las siguientes una o dos semanas). En caso de ataques leves, algunos clínicos prefieren tratamiento oral con 60 a 80 mg de prednisona por día o con 16 mg de dexametasona por día, administrados durante una semana con una reducción gradual rápida a lo largo de las siguientes dos semanas.
Pronóstico
- Es factible anticipar al menos una recuperación parcial de un episodio agudo, pero es imposible predecir cuándo sucederá una siguiente recurrencia. Las características que tienden a implicar un pronóstico más favorable incluyen sexo femenino, inicio antes de los 40 años de edad y presentación con disfunciones visuales o somatosensoriales, en lugar de piramidales o cerebelosas. Aunque es probable que se presente cierto grado de discapacidad a la larga, cerca de la mitad de todos los pacientes sólo presenta discapacidades leves o moderadas 10 años después de la presentación de los síntomas.
- MIELOPATÍAS VASCULARES Y TUMORES CON COMPRESIÓN MEDULAR
MIELOPATÍA TRAUMÁTICA
MIELOPATÍAS DESMIELINIZANTES
TUMORES Y COMPRENSIÓN MEDULAR
TUMORES Y COMPRESIÓN MEDULAR
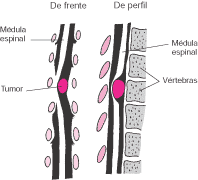
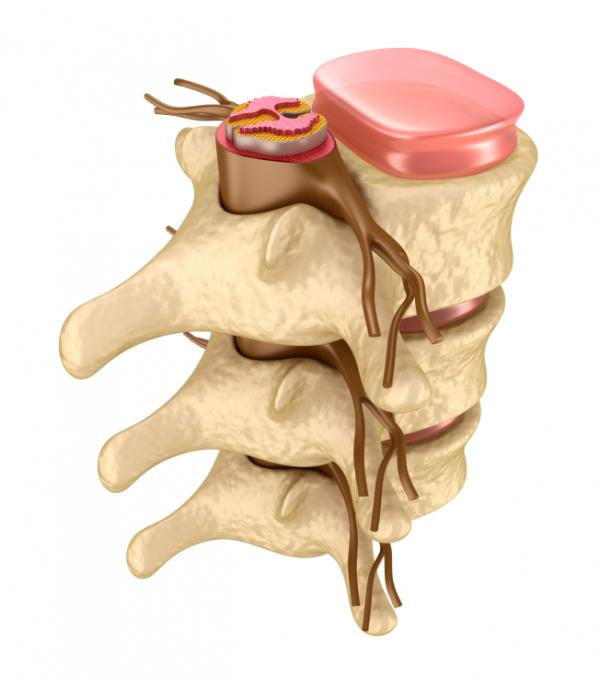
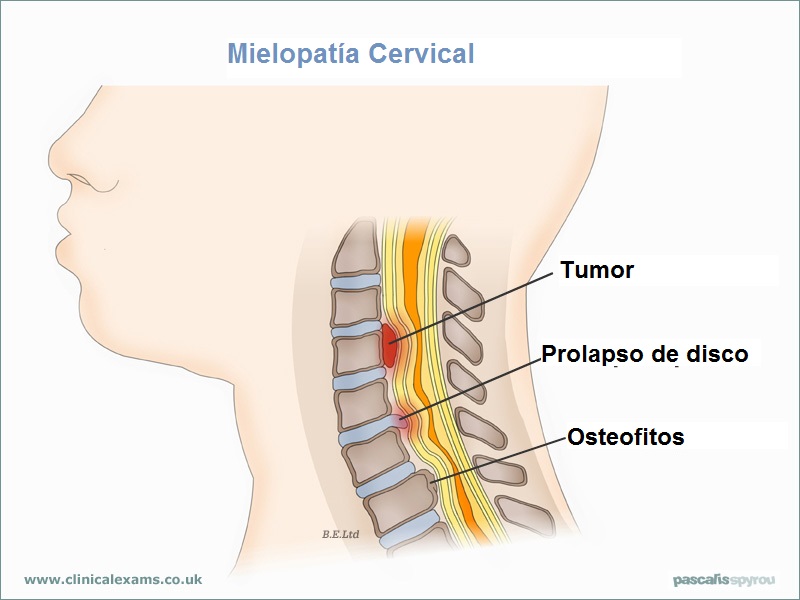
Las causas comunes de la compresión medular son protrusión de disco, traumatismo y tumores; en ciertas partes del mundo, la tuberculosis de la columna también es una causa frecuente. Causas inusuales, pero importantes, incluyen abscesos y hematomas epidurales. La presente sección se limitará a la consideración de tumores, y las causas adicionales se tratarán en otro sitio.
Clasificación
Los tumores se dividen en dos grupos: intramedulares (10%) y extramedulares (90%). Los ependimomas son el tipo más común de tumor intramedular y los diversos tipos de gliomas comprenden el resto. Los tumores extramedulares pueden ser de localización extradural o intradural. Entre los tumores extramedulares principales, los neurofi bromas y meningiomas son relativamente comunes y son benignos; pueden ser intra o extradurales. Por lo general, son extradurales las metástasis carcinomatosas (en especial las provenientes de los bronquios, mamas o próstata), depósitos linfomatosos o leucémicos y mielomas.
Hallazgos clínicos
Al margen de su naturaleza, un tumor puede conducir a una disfunción medular y a deficiencias neurológicas por medio de compresión directa, isquemia secundaria a obstrucción arterial o venosa o, en el caso de lesiones intramedulares, infiltración invasiva.
- Síntomas
Los síntomas se pueden desarrollar de manera insidiosa y progresar de manera gradual o como es frecuente con la compresión de la médula espinal a causa de un carcinoma metastásico exhibir un curso rápido.
El dolor es una característica evidente y por lo general la primera anormalidad en muchos pacientes con lesiones extradurales; puede ser radicular, limitado a la espalda, o experimentado de manera difusa en una extremidad y, de manera característica, se ve agravado al toser o hacer esfuerzos.
Llegan a desarrollarse síntomas motores (pesadez, debilidad, rigidez o emaciación focal en una o más extremidades) o presentarse parestesias o entumecimiento, en especial en las piernas. Cuando suceden alteraciones esfinterianas, por lo general son particularmente discapacitantes.
- Signos
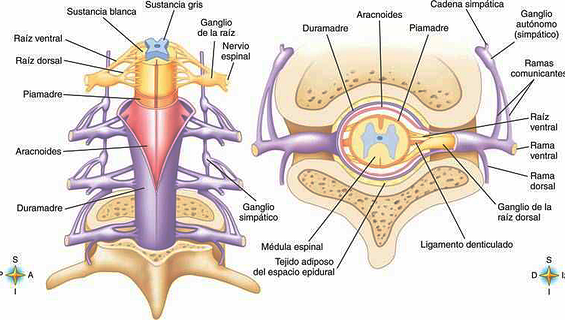
En ocasiones, la exploración revela sensibilidad espinal localizada ante la percusión. La afectación de las raíces anterioresconduce a una deficiencia apropiada de neurona motora inferior, y la afectación de las raíces posteriores conduce a cambios sensoriales dermatómicos al nivel de la lesión. El compromiso de las vías que atraviesan la médula puede ocasionar una deficiencia de neurona motora superior por debajo del nivel de la lesión y a una deficiencia sensorial con nivel superior en el tronco. La distribución de signos varía con el nivel de la lesión y en ocasiones toma la forma de un síndrome Brown-Séquard o central de la médula espinal.
Estudios de investigación
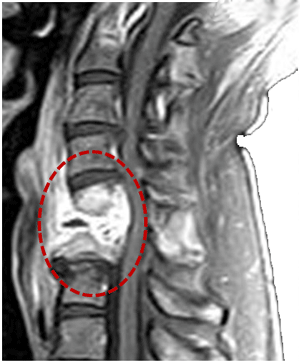
A menudo, el LCR es xantocrómico, con un aumento importante en la concentración proteínica, un conteo normal o elevado de leucocitos y una concentración de glucosa normal o elevada. Una radiografía simple de la columna puede o no mostrar anormalidades, y una exploración TC, IRM o mielografía son necesarios para delinear la lesión y localizarla de manera precisa.
Tratamiento
El tratamiento depende de la naturaleza de la lesión. Las metástasis extradurales deben tratarse de forma urgente. En función de la naturaleza del neoplasma primario, su mejor manejo se obtiene con analgésicos, corticosteroides, radioterapia y tratamientos hormonales; a menudo es innecesaria una laminectomía descompresiva. De ser posible, lo mejor es extirpar las lesiones intradurales (pero extramedulares). Los tumores intramedulares se tratan con descompresión y extirpación quirúrgica cuando es factible y con radioterapia.
Pronóstico
El pronóstico depende de la causa y gravedad de la compresión medular antes de aliviarse. Por lo general, la compresión medular ocasionada por metástasis extradurales se manifiesta de inicio únicamente con dolor y puede progresar con velocidad hasta causar alteraciones permanentes de las funciones motora, sensorial y esfi nteriana. Por ende, el diagnóstico debe sospecharse de inicio en pacientes con cáncer y con dolor vertebral o radicular y se debe investigar de inmediato. Si se espera a observar alteraciones motoras, sensoriales o esfinterianas para realizar el diagnóstico, el tratamiento se demorará de manera innecesaria y el pronóstico empeorará.
INFARTO DE LA MÉDULA ESPINAL.
Es un suceso inusual que ocurre de forma más común en el territorio de la arteria espinal anterior, la cual irriga las dos terceras partes anteriores de la médula, está irrigada en sí sólo por un número limitado de vasos de alimentación, mientras que el par de arterias espinales posteriores se ven irrigadas por diversos vasos de alimentación a muchos diferentes niveles.
- Así, por lo general, el síndrome de la arteria espinal anterior es el resultado de la interrupción de flujo de uno de sus alimentadores. Otros patrones de afectación incluyen patrones arteriales espinales unilaterales anteriores o posteriores, centrales y posteriores, así como un síndrome transversal. Las causas incluyen traumatismos, aneurisma aórtico disecante, aortografía, poliarteritis nodosa y crisis hipotensiva.
- Dado que la arteria espinal anterior se encuentra particularmente bien irrigada en la región cervical, los infartos casi siempre ocurren de manera más caudal. La típica presentación clínica del síndrome de arteria espinal anterior es un inicio agudo de una paraparesia flácida arrefléxica que, a medida que el choque espinal desaparece después de unos cuantos días o semanas, evoluciona a una paraparesia espástica con reflejos tendinosos enérgicos y respuestas de extensión plantar.
- Además, existe una alteración sensorial disociada; se pierden la apreciación de dolor y temperatura, pero quedan intactos el sentido de la vibración y posición a causa de que las columnas posteriores están irrigadas por las arterias espinales posteriores. El tratamiento es sintomático. En ocasiones, se desarrolla una mielopatía asimétrica subaguda como consecuencia de un proceso vasculítico; el LCR muestra una pleocitosis y se puede obtener un beneficio clínico de terapia esteroidea.
- Una mielopatía isquémica asimétrica aún más insidiosa puede relacionarse con la compresión de la arteria espinal anterior o de su vaso de alimentación principal, como en el caso de enfermedad degenerativa espinal. El trastorno resultante puede simular una esclerosis lateral amiotrófica cuando existe una deficiencia combinada de neurona motora superior e inferior, sin cambios sensoriales.
Hemorragia epidural o subdural
La hemorragia espinal epidural o subdural puede ocurrir en relación con traumatismo o tumor y como complicación por anticoagulación, terapia con aspirina, trombocitopenia, coagulopatía, catéteres epidurales o punción lumbar. De forma ocasional sucede de manera espontánea. La probabilidad de que ocurra una hemorragia posterior a una punción lumbar normalmente localizada en la región lumbar aumenta cuando existe un trastorno de la coagulación.
Por ende, se deben determinar el conteo de plaquetas, el tiempo de protrombina y el tiempo parcial de tromboplastina antes de llevar a cabo una punción lumbar y, si se ha de instituir terapia de anticoagulación, se debería demorar al menos una hora después del procedimiento. Los pacientes con menos de 20 000 plaquetas/ mm3 o aquellos con conteos en descenso rápido (hasta de 50 000) deberían ser transfundidos antes de una punción lumbar.
Por lo general, la hemorragia espinal epidural se presenta con dolor de espalda que puede irradiarse en la distribución de una o más raíces espinales nerviosas; en ocasiones, es indolora. Es posible que se desarrollen con velocidad paraparesias o cuadriparesias, alteraciones sensoriales de las extremidades inferiores y disfunción urinaria e intestinal, haciendo necesaria una urgente exploración con TC, IRM o mielografía y la evacuación del hematoma.
TUMORES Y COMPRENSIÓN MEDULAR